
Johannes Diderik Van Der Waals Amsterdam University Amsterdam, the Netherlands 1837 - 1923 |

Johannes Diderik Van Der Waals Amsterdam University Amsterdam, the Netherlands 1837 - 1923 |
Johannes Diderik van der Waals nasceu a 23 de Novembro de 1837 em Leyden. Era o filho mais velho de Jacobus van der Waals e de Elisabeth van den Burg numa família de oito irmãos. Foi um dos mais influentes físicos holandeses de considerável valor para o progresso da ciência na Holanda e para o prestígio da Holanda neste campo.
Após ter terminado a escolaridade básica van der Waals estudou para professor primário, profissão que veio a exercer entre 1856 e 1861 na sua terra natal. Efectuou estudos na Universidade de Leyden frequentando aulas de matemática, de física e de astronomia.
De 1864 foi professor numa escola secundária em Deventer e em 1866 mudou-se para The Hague onde ensinou Física e Matemática numa das escolas secundárias que também dirigiu.
Os conhecimentos de latim e grego constituiam por esta altura um prerequesito para a graduação académica. Embora van der Waals não possuisse tais conhecimentos continuou nos tempos livres a estudar na Universidade de Leyden entre 1862-65. Após uma revisão legislativa, os estudantes de ciência deixaram de depender do conhecimento das linguas clássicas e desta forma van der Waals conseguiu efectuar os exames universitários. Em 1873 J.D. van der Waals obteve o grau de Doutor com a defesa da tese "Over de continuïteit van de gas- en vloeistoftoestand" ("Acerca da continuidade dos estados gasoso e líquido "). Foi aqui que publicou a sua bem conhecida equação
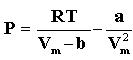
A origem do interesse de van der Waals pelo assunto abordado na sua tese terá sido um tratado da autoria de Rudolph Clausius onde o calor era considerado como um fenómeno provocado pelo movimento molecular. Estas ideias levaram van der Waals a procurar uma explicação para o andamento das isotérmicas no comportamento PVT de substâncias puras, encontradas por Andrews entre 1861 e 1869 as quais revelavam a existência de temperaturas críticas. Resultou a equação de estado proposta na base de que as moléculas ocupam um volume e exercem forças intermoleculares entre si (conhecidas como "forças de van der Waals"). A equação de estado de van der Waals permitia prever a condensação dos gases e o ponto crítico das substâncias - a transição do estado líquido para o gasoso e vice versa, ocorria de forma contínua.
Esta equação contituiu um avanço muito significativo relativamente à equação de estado dos gases perfeitos. A importância das conclusões obtidas por van der Waals foi apreciada por Maxwell num artigo publicado na Nature. Escrevia este ilustre cientista que " não pode haver dúvida de que o nome de van der Waals em breve estará entre os primeiros da ciência molecular".A contribuição de van der Waals foi de tal forma importante que subsequentemente numerosos artigos foram publicados nesta área nos Proceedings of the Royal Academy of Sciences e nos Archives Néerlandaises, com tradução em várias linguas.Em 1876 após a saída de nova legislação sobre o ensino superior o Athenaeum Illustre de Amsterdão ganhou estatuto universitário e van der Waals tornou-se o primeiro professor de Física e durante os primeiros anos o único responsável pelo ensino desta disciplina na Universidade "Illustre"de Amsterdão. Conjuntamente com Van't Hoff entre outros, contribuiu para a fama da universidade e aí se manteve até à reforma apesar de ter recebido convites de várias instituições.
Nos anos que se seguiram a 1873 van der Waals deu contribuições importantes à Física. Em 1880 formulou a "Lei dos Estados Correspondentes", em 1890 desenvolveu a sua teoria acerca do comportamento das misturas binárias e em 1893 a teoria dos fenómenos capilares.
A lei dos estados correspondentes estabelecia que, desde que fossem defenidas variáveis (reduzidas) para a pressão, volume e temperatura, podia obter-se uma equação de estado aplicável a todas as substâncias - nestas condições as costantes a, b e R na equação de estado de VDW que podiam ser expressas em termos das propriedades críticas da substância, desapareciam. Foi esta lei que guiou J. Dewar nas experiências que culminaram com a liquefação do hidrogénio em 1898 e do hélio por Kamerlingh Onnes em 1908. K. Onnes que recebeu o Prémio Nobel em 1913 pelos seus estudos no domínio das baixas temperaturas e pela produção do hélio líquido escreveu em 1910 que sempre tinha considerado que os estudos de van der Waals eram uma espécie de mão mágica na realização das suas experiências e que o seu laboratório de criogenia em Leyden se desenvolveu sob a influência das suas teorias. Os conselhos teóricos de van der Waals terão valido de algum modo a Kamerlingh Onnes nos trabalhos por este realizados no campo da liquefação dos gases. Aliás van der Waals fez parte de uma comissão do Governo encarregada de estudar o problema de segurança do Laboratório de Kamerlingh Onnes levantado por alguém junto do ministro do Interior.Esta comissão deu um parecer positivo sobre as condições de segurança usadas no laboratório de Leyden graças à intervenção de van der Waals.
Em 1890 apareceu nos Archives Néerlandaises o primeiro tratado sobre "Teoria das soluções binárias" Esta teoria nasceu da relação que van der Waals conseguiu estabelecer entre a sua equação de estado e a formulação do 2º Princípio da Termodinâmica na forma proposta por W. Gibbs.
Van der Waals recebeu vários prémios, honras e distinções.Foi Doutor Honoris Causa pela Universidade de Cambridge, membro honorário da Sociedade Imperial Russa de Naturalistas (Moscovo), da Real Academia Irlandesa e da American Philosophical Society. Foi membro correspondente do Institut de France e da Royal Academy of Sciences (Berlin) e membro da Academia Real das Ciências da Bélgica, da Chemical Society of London, da National Academy of Sciences of the U.S.A. e da Accademia dei Lincei of Rome. Era um dos únicos doze membros estrangeiros da Academia de Ciências de Paris.De 1875 a 1895 Van der Waals foi membro da Real Academia Holandesa da Ciência "Koninklijke Academie van Wetenschappen".
van der Waals reformou-se em 1908, com a idade de 71 anos. Em 18 de Novembro do mesmo ano conjuntamente com Kamerlingh Onnes foi galardoado em Amesterdão com a medalha de ouro da "Genootschap ter bevordering van natuur-, genees- en heelkunde" (Sociedade para o benefício da Física, Ciência médica e cirúrgica): era uma grande honra receber esta distinção. Em 1910 recebeu o Prémio Nobel da Física pelo trabalho efectuado no domínio das equações de estado de gases e fluídos.Após Kamerlingh Onnes, Zeeman, Lorentz e Van 't Hoff van der Waals foi o quinto físico holandês a receber o Nobel.
van der Waals casou em 1864 com Anna Magdalena Smit. Após a morte prematura da esposa van der Waals não voltou a casar. Do casamento nasceram três filhas e um filho: Anne Madeleine dedicou-se ás tarefas da casa e ao cuidado do pai após a morte da mãe; Jacqueline Elisabeth foi professora de História e uma poetisa de nomeada; Johanna Diderica foi professora de Inglês. Johannes Diderik Jr. foi professor de Física na Universidade de Groningen entre 1903 e 1908, sucedendo a seu pai na cadeira de Física lecionada na Universidade de Amsterdão.
Andar no campo e a leitura eram duas coisas que Van der Waals fazia com grande prazer.
Van der Waals faleceu em Amsterdão dia 8 de Março de 1923 com a idade de 85 anos. O seu trabalho frutificou e continua a ser uma forte fonte de inspiração ainda nos nossos dias.
Bibliografia
K. Mendelssohn " Em demanda do zero absoluto", World University Library, 1968
Nobel Lectures, Elsevier Publishing Company, Amsterdam, 1964-1970
| As
Nobel Lectures são no seu conjunto um trabalho constituído pelas comunicações Nobel desde 1901, com notas biográficas,
referências a prémios e discursos de apresentação sendo todo este material
autorizado pela Fundação Nobel. Inclui os seguintes volumes: Física, 1901-1970, 4 vols. Química, 1901-1970, 4 vols. Fisiologia e Medicina , 1901-1970, 4 vols. Literatura, 1901-1967, 1 vol. Paz, 1901-1970, 3 vols. Após 1970 a editora Elsevier decidiu por não continuar as series. |