|
|
Determinacão de equilíbrio líquido-vapor (L-V) por métodos heterogéneos
Considere-se um sistema de N componentes constituído por uma fase liquída em equilíbrio com a fase gasosa à temperatura T e à pressão P. A composição da fase líquida é dada pelas fracções molares (x1,x2, xN) e a da fase gasosa por (y1,y2, yN). As equações da termodinâmica que traduzem o equilíbrio entre as fases líquida e gasosa num sistema de N componentes, são
|
|
onde fi designa a fugacidade do componente i na mistura. Tendo em conta que
|
|
onde f i designa o coeficiente de fugacidade do componente i na mistura gasosa, e
|
|
onde g i designa o coeficiente de actividade do componente i na fase líquida e Pis é a pressão de vapor do componente i à temperatura T. Deste modo
|
|
Ao todo existem 2N variáveis em jogo (N-1 fracções molares para a fase líquida, N-1 fracções molares para a fase gasosa, P e T- quer dizer 2(N-1)+2 = 2N variáveis - e temos N equações da forma (4). Assim, num dado problema de cálculo de equilíbrio líquido-vapor (ELV) é necessário fixar o valor de N variáveis (propriedades) enquanto que os valores das restantes N variáveis (propriedades) são determinados pelas N equações do tipo (4). Relativamente à depedência do coeficiente de actividade e do coeficiente de fugacidade em termos de P, T e composição temos que
|
| e |
e, consequentemente a resolução de problemas de ELV é feita recorrendo a técnicas de iteração. Os problemas de cálculo que se podem colocar são:
|
PROPRIEDADES FIXAS |
PROPRIEDADES A DETERMINAR |
IDENTIFICAÇÃO DO PROBLEMA |
|
T, xi |
P, yi |
BUBL P |
|
P, xi |
T, yi |
BUBL T |
|
T, yi |
P, xi |
DEW P |
|
P,yi |
T, xi |
DEW T |
Existe outro tipo de problema que é o cálculo FLASH, tratado numa secção própria. (veja CÁLCULO FLASH)
1 - CÁLCULOS DE BUBL P e BUBL TExplicitando (4) em ordem a yi,
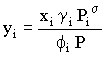 |
quer dizer
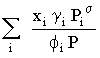 | porque |
ou, também
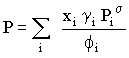 |
A equação anterior pode ainda escrever-se
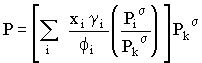 |
onde Pks é a pressão de vapor de um componente puro k, à temperatura T de equilíbrio. Podemos também escrever
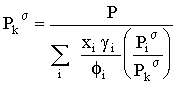 |
Dada uma equação da pressão de vapor para o componente k, genéricamente do tipo Pks = f (T) ela pode ser resolvida em ordem a T sabendo P. Uma forma conveniente que permite uma rápida explicitação em T é a conhecida equação de Antoine,
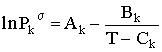 | 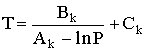 |
As equações (5) a (8) são utilizadas em cálculos de BUBL P e BUBL T :
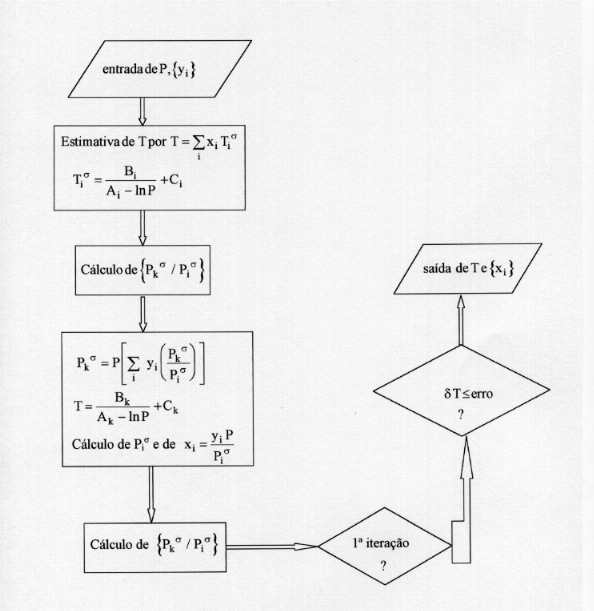
1.1 - CÁLCULOS DE BUBL P
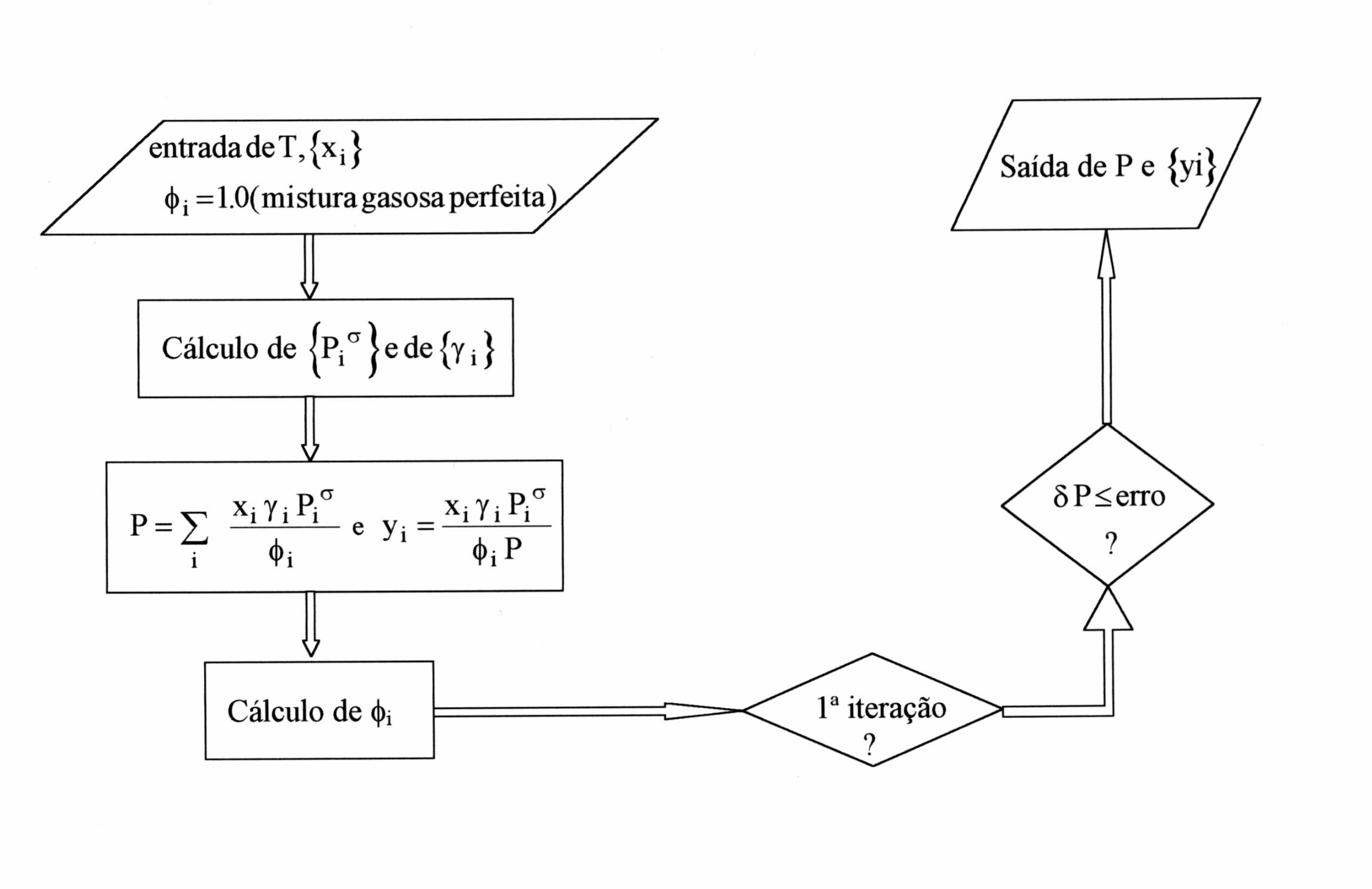
O valor de d P poderá ser da ordem de 0.0001 kPa para cálculos realizados em PC's.
Para o caso da lei de Raoult f i =1(mistura gasosa perfeita) e g i=1 (solução ideal)
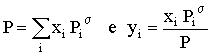 |
1.2 - CÁLCULOS DE BUBL T
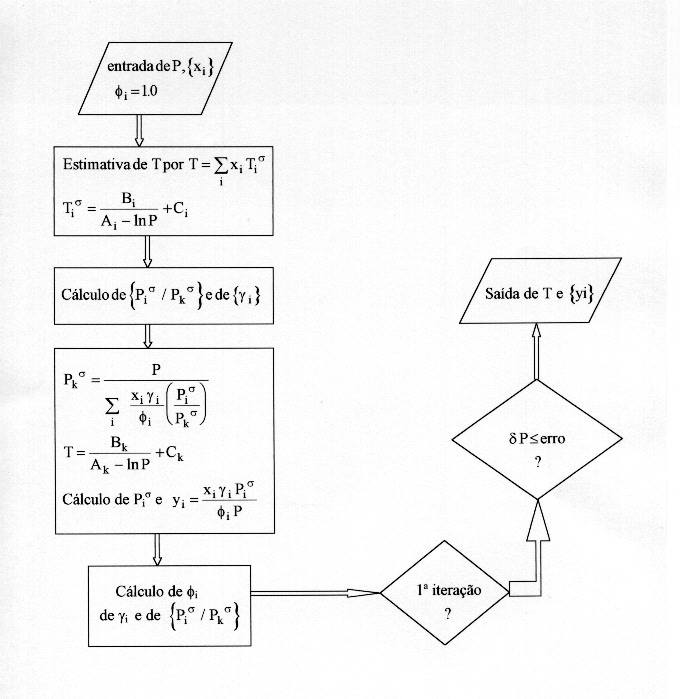
Para o caso da lei de Raoult:
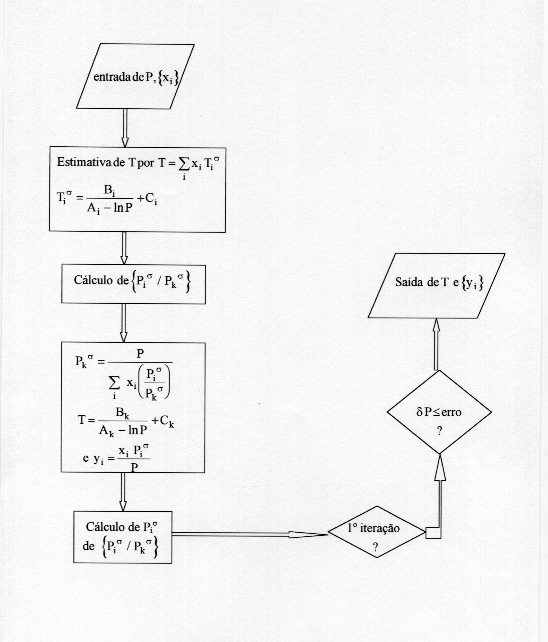
2 - CÁLCULOS DE DEW P e DEW T
Resolvendo (4) em ordem a xi
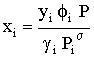 |
Quer dizer
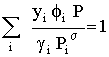 |
ou, também
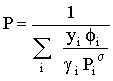 |
A equação anterior pode ainda escrever-se
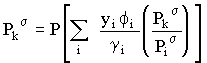 |
e, da mesma forma que anteriormente
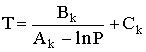 |
As equações (8) a (11) são utilizadas em cálculos de DEW P e DEW T:
2.1 - CÀLCULOS DE DEW P
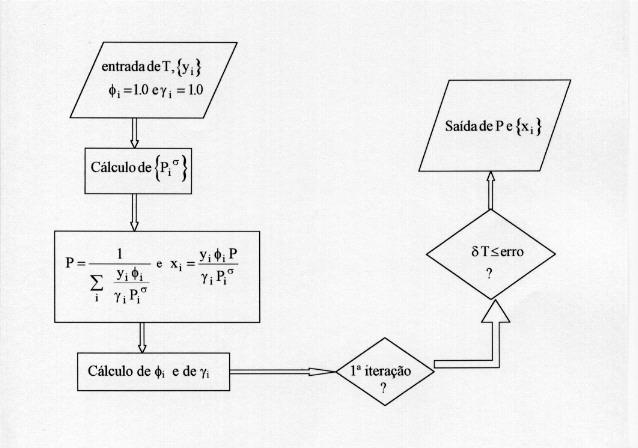
Para o caso da lei de Raoult:
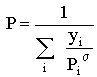 | 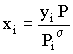 |
2.2 - CÀLCULOS DE DEW T
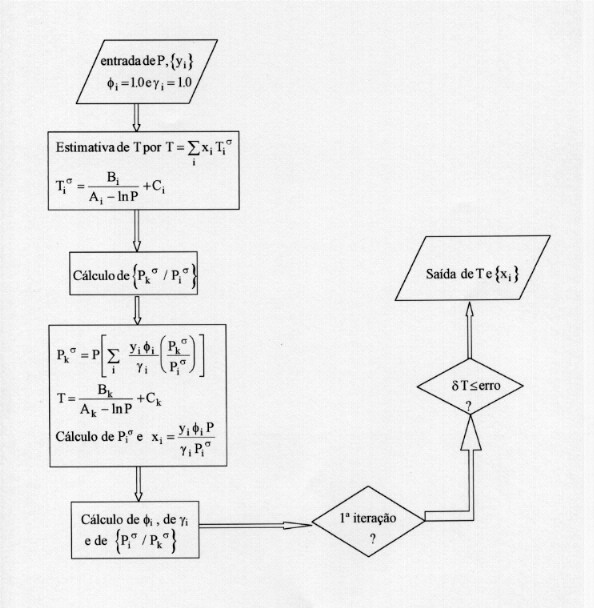
Para o caso da lei de Raoult :