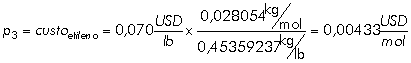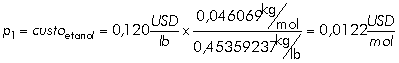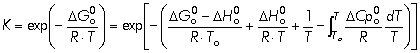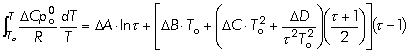|
|
6 |
CASE STUDY –
Produção de Etanol |
|
|
|
|
|
As três vias que iremos comparar são
descritas pelas seguintes reacções:
Com a metodologia que apresentamos
neste trabalho de seminário, pretendemos olhar para a transformação
química na sua essência. Iremos então concentrar-nos na transformação
que nela ocorre não só do ponto de vista químico, mas também nas vertentes
económica e ambiental. Pois se num processo, um input de ik
moles se transforma num output de ok moles, também os valores
económico e ambiental destas k substâncias, sofrem uma mudança Dpk e Dak, respectivamente.
Fig. 6.8 – Transformação química,
económica e ambiental das k substâncias.
Temos portanto dois objectivos: o desempenho
económico (DE) e o desempenho ambiental (DA) da transformação.
O desempenho económico (DE)
em USD pode, numa primeira abordagem, ser descrito de uma forma simplificada,
como a diferença entre valor económico de input e output. Para o processo
A (hidratação directa do etileno), temos então:
Note-se que nesta fase da nossa abordagem,
o processo está completamente em aberto – não sabemos que tipo de equipamento
vamos usar, que flowsheet, etc. Vamos considerar apenas a “transformação
química” em si. Este tipo de abordagem é comum sempre que se começa
por estudar uma “ideia de processo”. Por isso mesmo, o valor económico
de uma substância vai ser considerado constante, independentemente quer
ela esteja presente numa corrente pura ou numa mistura com outros componentes.
Note-se apenas que o preço de catalisador p4 é expresso em
USD/mol de etanol formado.
De forma análoga o desempenho ambiental
(DA) associado à transformação química pode ser descrito usando, em
vez dos valores económicos pk, valores ambientais expressos
em unidades de impacte por mol, ak. A única diferença é que
iremos definir DA como a diferença entre o início e o fim, e não entre
o fim e o início. Deste modo, se o impacte ambiental diminuir, DA será
positivo. Se o impacte ambiental aumentar, DA será negativo.
Os valores económicos assumem-se como
os preços industriais das substâncias químicas, que se retiraram do
Chemical Market Reporter[6.3], edição de Março de 2003. Temos
então, a título ilustrativo:
O preço da água industrial desmineralizada
é pequeno face aos das outras substâncias [6.5]:
O catalisador custa 5USD/ton etanol[6.1].
Pelas moles de etanol conseguidas paga-se portanto:
O preço refere-se no entanto ao ano
de 1989, daí ser necessário actualizá-lo. Para tal iremos recorrer ao
Chemical Engineering Cost Plant Index, compilado pela revista Chemical
Engineering[6.6]:
Quanto aos valores ambientais ak,
estes correspondem aos índices PEI convertidos para unidades de impacte
por mol. Finalmente, após cerca de 8 anos, os investigadores da US/EPA
que criaram os índices tomaram a decisão de tornar acessível a base
de dados desenvolvida e que possui os PEI de mais de 6000 substâncias.
Isto só é no entanto possível através de um simulador de processos:
o ChemCAD.
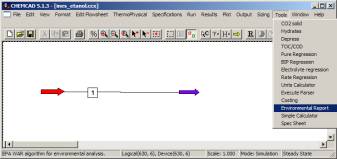
E se o acesso à base de dados a partir
do programa não é imediato, é possível contornar os obstáculos. Para
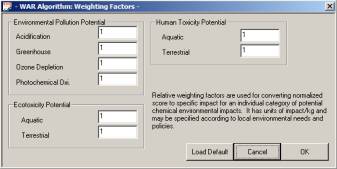
se visualizar os PEI é necessário criar uma corrente, à qual, por simplicidade
se atribui um caudal unitário (1kg/h) a cada substância. A opção “Environmental
Report” leva-nos à análise do flowsheet através do algoritmo WAR. Como
o nosso flowsheet é composto apenas por uma corrente, obtemos assim
a lista de impacte das substâncias que compõem a corrente em unidades
de impacte/h, que correspondem a impacte/kg porque os caudais são unitários.
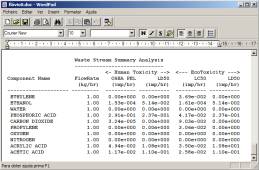
Fig. 6.8 – Obtenção no ChemCAD 5 dos valores dos PEI de substâncias presentes numa corrente, através da opção “Environmental Report”.
Os índices vêm discriminados segundo
8 categorias de impacte ambiental: depleção do ozono, efeito de estufa,
formação de smog, chuva ácida, toxicidade humana (OSHA PEL e LD50),
e ecotoxicidade (LC50 e LD50).
Tab. 6.1 – “Environmental Report”
gerado pelo ChemCAD 5.
Neste trabalho iremos dar, por simplicidade,
ponderação igual a todas as categorias (contudo, é procedimento frequente dar-se muitas vezes
maior ponderação à toxicidade humana, p.ex.). Assim sendo, para uma
dada substância, o PEI corresponde ao somatório dos resultados de cada
categoria.
Tab. 6.2 – Valores ambientais
ak e valores do índice PEI (Potential Environmental Impact
Index) para algumas substâncias.
Pelo
que, a título ilustrativo, temos:
6.3 – Optimização
Para o caso específico da hidratação
directa, encontraram-se dados cinéticos disponíveis que permitem fazer
uma optimização das condições operatórias conducentes ao maior desempenho
económico e ambiental.
Em linguagem de optimização, temos
pela frente um problema de programação não linear (NLP – Non Linear
Programming), que pode ser definido da seguinte forma[6.7]:
Para conhecer as dependências dos desempenhos
DE e DA com as variáveis independentes (pressão, temperatura, e moles
de reagentes iniciais) é necessário recorrer a dados cinéticos e termodinâmicos.
Começamos por apresentar já de uma
forma condensada alguns dos dados que serão necessários:
Tab. 6.3 – Compilação de valores
de propriedades em jogo.
A
reacção dá-se em fase gasosa homogénea, sendo por isso a relação de
equilíbrio: [6.4]
Como
o coeficiente estequeométrico global é
Então:
As fugacidades fk podem ser estimadas como funções da temperatura
reduzida Tr=T/Tc e do factor acênctrico w[6.4]:
Por
outro lado:
Pelo
que:
Já
o cálculo da constante de equilíbrio pode ser estimado, no caso desta
reacção, pela equação[6.4]:
Assumindo
que
Com:
To=298,15K é a temperatura de referência
Validade das equações: 298,15K<T<1500K
Temos
ainda que:
A
equação (6.1), em associação com as (6.2,3,4) fica assim na forma:
Para
terminar, interessa-nos explicitar a coordenada genérica de reacção
e:
Face a isto podemos proceder à fase
seguinte: optimização das nossas funções objectivo desempenho económico
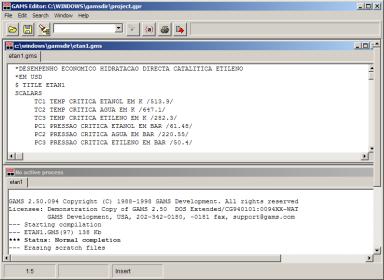
e ambiental. Para tal usou-se o software de optimização GAMS-IDE.
Fig. 6.9 – Splashscreen do
software usado no capítulo da optimização: GAMSIDE 1.0.4.
A transcrição desta formulação matemática
para código de programação em GAMS é simples, e encontra-se no anexo
I.
As condições óptimas de operação a
que se chegou foram: T=718K, P=70bar, e
i2/i3=0,61 moles de água por mol de etileno
na alimentação, que conduzem a uma conversão de etileno de cerca de
4,03%. Estas estão em relativo acordo com os valores que se praticam
na realidade industrial, à excepção da temperatura que é um bocado maior.
Este capítulo da optimização vinha
complementar as análises económica e ambiental e torná-las mais completas,
uma vez que se entraria em conta com a taxa de conversão de reagentes
em cada caso, e as alterações subsequentes em termos económicos e ambientais.
No entanto, não foi possível desenvolver as mesmas formulações para
as outras 2 vias (hidratação indirecta e fermentação), por falta de
informação disponível. Assim sendo, a comparação económica e ambiental
que se segue será feita com base na estequeometria da reacção, tendo
por base de cálculo 1 mol de produto etanol.
6.4 – Comparação Económica e Ambiental
Análise
Ambiental
Começaremos por uma análise ambiental.
Antes de mais, interessa saber qual o valor em impacte por mol associado
a cada uma das substâncias envolvidas neste case study.
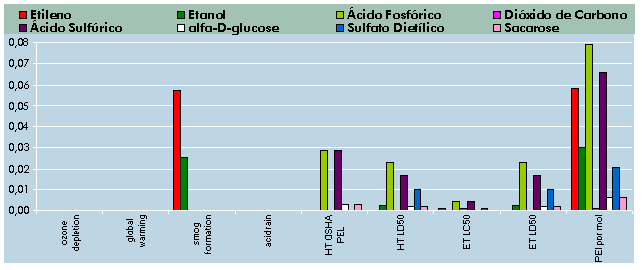
Fig. 6.10 – Contribuição das
várias categorias de impacte ambiental no valor do Índice PEI (em unidades
de impacte por mol).
Claramente, as categorias de impacte
ambiental mais afectadas são a formação de smog, a toxicidade humana
(HT-OSHA PEL e HT-LD50) e ecotoxicidade (ET-LC50 e ET-LD50). No campo
das toxicidades, destacam-se o ácido sulfúrico (reagente na hidratação
indirecta) e o ácido fosfórico (catalisador na hidratação directa).
O etileno revela uma contribuição muito significativa como factor de
formação de smog. Dentro dos reagentes, o maior valor de impacte ambiental
por mol vai para o ácido sulfúrico em 1º lugar (hidratação indirecta)
e para o etileno em 2º (hidratação directa). Na lista de produtos, o
etanol é 1º e o CO2 2º (fermentação). Resta o catalisador
ácido fosfórico que, apesar de estar presente em pequenas quantidades
no processo, possui grandes toxicidades. Refira-se para terminar que
neste gráfico não está incluída a água porque esta possui um valor nulo
de impacte ambiental.
O
passo seguinte é analisar o que acontece à variação de impacte ambiental
em cada uma das 3 vias de produção, ou seja, o desempenho ambiental
DA. Vamos então definir uma base comum às 3 vias – 1 mol de etanol produzida:
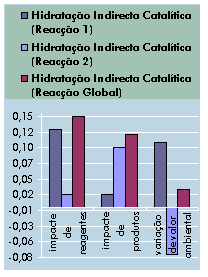
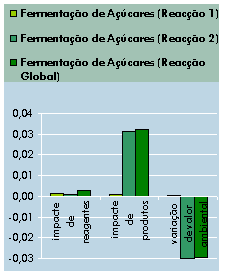
Impacte de reagentes, produtos, e variação
de impacte (unidades: impacte ambiental)
Fig. 6.11 – Valor ambiental de produtos e reagentes, e
sua variação (base de cálculo: 1 mol de etanol formado).
Concluímos então que, por cada mol
de etanol formada, a variação de impacte ambiental é:
- a hidratação
directa envolve uma melhoria ambiental de 0,028 unidades de impacte. - a hidratação
indirecta envolve uma melhoria ambiental de 0,027 unidades de impacte. - a fermentação
envolve uma pioria ambiental de 0,030 unidades de impacte.
Isto permite afirmar que nas duas vias
sintéticas (hidratação directa e indirecta) há uma valorização das substâncias
químicas, uma vez que os reagentes possuem maior impacte ambiental que
os produtos. Na fermentação acontece o contrário.
No entanto, é um dado que pode ser
complementado com outros, também relevantes, como a quantidade de impacte
associada aos reagentes e a quantidade de impacte associada aos produtos,
quando se forma 1 mol de etanol. Na verdade, o impacte ambiental dos
produtos finais é, por cada mol de etanol formada:
- para a hidratação
directa, 0,030 unidades de impacte. - para a hidratação
indirecta, 0,116 unidades de impacte. - para a fermentação,
0,032 unidades de impacte.
O impacte ambiental dos reagentes
que se vão buscar, por 1 mol de etanol formada é:
- para a hidratação
directa, 0,059 unidades de impacte. - para a hidratação
indirecta, 0,145 unidades de impacte. - para a fermentação,
0,003 unidades de impacte.
Podemos seriar estes dados sabendo
que em 1º lugar (melhor opção) fica a via que possuir maior valorização
ambiental, menor impacte de produtos, menor impacte de reagentes. Resumindo,
para cada via, as posições são as seguintes:
Tab. 6.4 – Seriação das 3 vias
segundo 3 critérios: impacte médio de reagentes, produtos, e valorização
ambiental.
Face a estes três critérios possíveis
qual será então o critério de decisão?
A valorização ambiental é sem dúvida
muito importante: está-se, no decurso da transformação química, a diminuir
o impacte ambiental dos inputs do processo. Neste capítulo, a hidratação
directa do etileno é a melhor classificada. Há, no entanto, que compreender
que, ao se implementar um processo de larga escala, se pode estar a
criar uma necessidade de mercado: no caso da hidratação directa, estariam
a criar-se condições para que a oferta de etileno no mercado fosse maior,
sendo o etileno um reagente de impacte ambiental alto. Nesta lógica,
a opção responsável seria optar pela via que possuísse reagentes de
mais baixo impacte ambiental (entre as 3, é inequivocamente a fermentação).
Haveria ainda outras considerações,
não no domínio ambiental, mas no domínio do risco: se uma dada
via envolve substâncias com maior impacte ambiental, e se considerarmos
que ao concretizarmos o processo na construção de uma fábrica, haverá
sempre risco de fugas para o meio ambiente e risco de fugas para zonas
onde estão trabalhadores, então importa também que as substâncias envolvidas
tenham baixo impacte ambiental. Neste caso, seria mais favorável optar
pela fermentação e não pela hidratação directa (ambas possuem o mesmo
impacte de produtos, mas a 2ª possui reagentes de elevado impacte).
Neste caso, uma proposta de critério de decisão poderia ser a menor
média dos valores de impacte ambiental ak de todas substâncias
envolvidas em cada via, ponderadas com a constante estequeométrica nk que possuem na reacção, em valor absoluto,
ou seja:
Neste case study, como pretendemos
apenas estudar o ponto de vista ambiental, iremos considerar que o critério
de decisão é a valorização ambiental. O melhor processo é então a hidratação
directa.
Análise
Económica
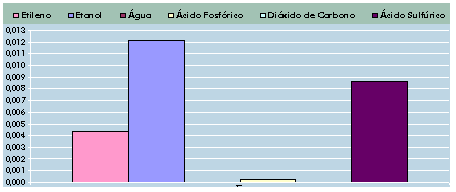
Os preços em USD por mol de algumas
das substâncias envolvidas encontram-se representados no gráfico abaixo.
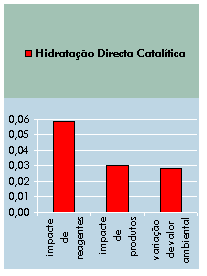
Valor
Económico (unidades:
USD/mol) Fig. 6.12 – Valor económico,
em USD, das substâncias envolvidas.
Do Chemical Market Reporter[6.3]
é possível estimar ainda
o preço do etanol produzido por fermentação. Segundo dados recentes,
o valor médio será 0,90 USD/galão de etanol. Isto corresponde a 0,90USD/(3,785x10-3m3x791kgm-3x0,046069molkg-1)=0,0138USD/mol
etanol.
Note-se que estas conclusões não reflectem
a realidade: o processo de fermentação na verdade é algo mais caro que
o da hidratação directa. Naturalmente, a incongruência pode dever-se
à abordagem simplista que estamos a efectuar e que não considera custos
de equipamento, operação, etc.
Solução
de Compromisso
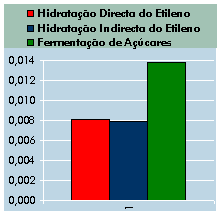
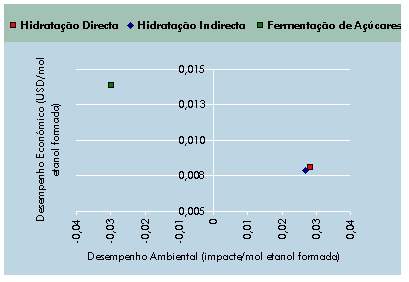
Se analisarmos as nossas três hipóteses
de produção do ponto de vista do desempenho ambiental (sendo o critério
a valorização ambiental, DA) e económico (DE) da transformação por mol
de etanol, obtemos o gráfico seguinte:
Fig. 6.14 – DE versus DA.
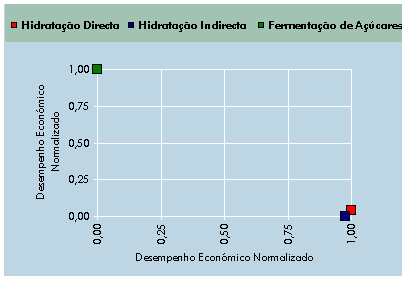
Este gráfico pode ser normalizado,
em ambas as categorias, se supusermos que o maior valor corresponde
a 100% e o menor a 0%:
Fig. 6.15 – DE normalizado
versus DA normalizado.
Estamos agora perante um dilema: por
um lado teríamos uma solução melhor economicamente e pior ambientalmente,
por outro teríamos uma 2ª solução com menos pontos económicos e mais
pontos ambientais. Entramos no campo das soluções de compromisso. Uma
das formas de fazer isto é atribuir uma ponderação a cada um dos critérios
e dizer que a minha solução é a Via x tal que
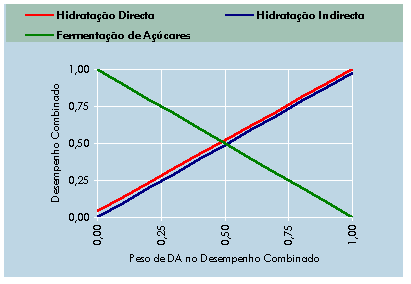
Vamos então calcular o valor do desempenho
combinado para várias ponderações possíveis, em que o peso do critério
ambiental pode ir de 0 a 1, e se considera que o peso do critério económico
é o valor complementar QE = 1- QA.
Fig. 6.16 – Valores do Desempenho
Combinado para diferentes ponderações do desempenho ambiental.
É agora mais simples optar por uma
das soluções. Como o critério económico é mais importante que o ambiental
(pelo menos do ponto de vista de quem vai “pagar” o processo), e tendo
em conta que uma ponderação aceitável do factor ambiental não será superior
a 50%, podemos dizer que a fermentação é o processo escolhido,
que combina melhor desempenho económico com ambiental. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Bibliografia [6.1] Chauvel, A. E Lefebvre, G.; Petrochemical Processes –
Technical and Economic Characteristics, Part II Major Oxygenated, Chlorinated
and Nitrated Derivatives; Gulf Publishing Company, Paris (1989); ISBN
0-87201-782-2; J31. [6.2]
López-Silva, A. et al; Processo de
Fabricación de bioetanol; Ingenieria Quimica, 391, Jun 2002. [6.3]
Chemical Market Reporter – Prices & People – Chemical Industry Prices;
24 Março 2003; www.chemicalmarketreporter.com/. [6.4]
Smith, J. et al; Introduction to Chemical Engineering Thermodynamics; (5ª
ed.) McGraw-Hill Int., Singapura (1996). [6.5] Departamento
de Engenharia Química do Instituto Superior Técnico; Preços de Utilidades
2002 - Dimensionamento e Optimização de Equipamentos e Utilidades: http://dequim.ist.utl.pt/doe/DOEU/Utilidades2002.pdf [6.6]
Chemical Engineering Magazine – Chemical Engineering Cost Plant Index
- http://www.che.com/ [6.7] Tavares, L.
e Correia, F; Optimização Linear e Não Linear – Conceitos, Algoritmos e
Métodos; 2ª ed., Fundação Calouste Gulbenkian, Lisboa (1999). [6.8]
Ethanol – driving towards a greener future; Ethanol History; http://www.ethanol-crfa.ca/history.htm [6.9] Instituto Geológico
e Mineiro – Relatório Síntese do 1º Fórum sobre Energias Renováveis
em Portugal; http://www.igm.pt [6.10]
Historic Ethanol Production / US Energy Information - http://bennelson.senate.gov/Historic%20Ethanol%20Production%20Chart.jpg
|
[
Custos e Impactes Ambientais no Projecto de Processos Químicos ]
[
Âmbito do Trabalho ]
[ Enquadramento da Questão Ambiental ]
[ Indicadores para Análise Ambiental ]
[
Ferramentas para Análise Ambiental de Processos Químicos
] [ Projecto de Caminhos
Reaccionais ]
[
CASE STUDY - Produção de Etanol ]
[ Conclusões ]
[ Nomenclatura ]