|
|
6 |
CASE STUDY –
Produção de Etanol |
|
|
|
|
O etanol (ou álcool etílico) é um líquido
incolor (o ponto de ebulição é 78ºC), com cheiro característico, volátil,
inflamável e solúvel em água. É utilizado como solvente no fabrico de
tintas, lacas, vernizes e perfumes, como combustível e na preparação
de produtos farmacêuticos. É ainda muito usado como desinfectante e
é comercializado sob a forma de álcool etílico a 96%, isto é, uma mistura
de 96 partes de álcool com 4 partes de água. É também usado como fluido
térmico em termómetros abaixo dos -40ºC, por possuir um baixo ponto
de fusão: -144,1ºC. É ainda produto de partida para várias sínteses
orgânicas: por oxidação origina o acetaldeído e depois ácido acético,
pode ser desidratado para dar éter e pode ser usado na síntese do butadieno,
do qual se faz a borracha sintética. Tal como todos os álcoois, o etanol
não existe livre na Natureza. O processo mais fácil de o obter é por
fermentação alcoólica da glucose, havendo ainda processos de síntese
a partir do etileno.
Fig. 6.2 – Mostras da presença
do etanol no nosso mundo – circo, bebidas, transportes, culinária, cosmética,
sínteses orgânicas, medicina.
Entre todas estas aplicações, há uma
que se tem tornado cada vez mais importante. O facto de esta molécula
ter 1 átomo de oxigénio torna-a num combustível de alta qualidade. A
combustão é mais completa e as emissões de CO são menores.
Já em 1908 o etanol foi o combustível
de eleição de Henry Ford, no emblemático carro Ford T.[6.8]
Nas décadas subsequentes, a descoberta de poços de petróleo nos E.U.A.
condicionou o desenvolvimento dos primeiros motores automóveis para
o uso da gasolina, e mais tarde do diesel. Hoje conhecem-se os problemas
ambientais associados a estas opções, a nível das emissões gasosas.
Na década de 70, e devido ao embargo da OPEC, o etanol reemergiu num
programa do Governo Federal Americano destinado a minorar a dependência
do petróleo estrangeiro e a fomentar a economia agrícola. Desde os anos
80 até agora, tem-se difundido o uso de gasolina misturada com etanol
um pouco por todo o mundo. Isto porque esta mistura pode ser usada em
qualquer automóvel posterior a 1970, sem qualquer alteração no motor.
Existem misturas pobres em etanol (E10 – 10% etanol e 90% gasolina)
e misturas ricas (E85 – 85% etanol e 15% gasolina)
Algumas vantagens do etanol são:
-
proveniência de fontes renováveis (o processo de fabrico mais frequente
é a fermentação). -
menores emissões de gases de estufa como o monóxido de carbono (redução
de 4% para o E10 e 37% para o E85). Isto é particularmente importante
porque 50% dos gases de estufa na terra provêm da utilização automóvel. -
menor contributo para o smog, porque os gases de escape são menos reactivos
e a formação de ozono de baixa altitude é menor (este ozono é prejudicial,
ao contrário do ozono estratosférico, e responsável por problemas respiratórios
humanos e das plantas). -
motores de combustão mais ecológicos, com menos depósitos. -
melhor performance do veículo, aumenta o nível de octanas (o E10 tem
94 octanas) e oxigénio, e a combustão dá-se a temperaturas menores (aliás,
os veículos de alta competição usam etanol puro). -
menor dependência de reservas petrolíferas -
desenvolvimento económico rural. -
substitui compostos perigosos da gasolina, ex: benzeno, tornando-a mais
segura ambientalmente: se a gasolina contaminar o solo ou água, o etanol
é naturalmente biodegradável
Por cá, na Europa, a Comunidade Europeia
tem advogado e promovido os biocombustíveis. Os Estados-Membros devem[6.9]: 1)
assegurar a promoção de uma quota de mercado de 7% para os biocombustíveis
em 2010; 2)
encorajar a redução do diferencial de preços entre os biocombustíveis
e os combustíveis tradicionais; 3)
incrementar a promoção voluntária da distribuição dos biocombustíveis
em larga escala pelas companhias petrolíferas; 4)
intensificar os esforços de pesquisa neste sector.
De entre os biocombustíveis disponíveis
contam-se: etanol e metanol, os seus derivados (ETBE – éter etil-tert-butílico e MTBE) e os ésteres metílicos
de óleos vegetais (girassol, colza, etc.), sendo os primeiros utilizados
em motores Otto de combustão e os segundos em motores Diesel.
O MTBE é um éter sintético usado desde
1979 nas gasolinas sem chumbo, podendo ter teores de 11%. É um oxigenante,
contribuindo para a combustão mais completa da gasolina (aumenta o índice
de octanas) e por isso leva a reduções nas emissões de poluentes atmosféricos,
como o CO e alguns percursores do ozono. Hoje sabe-se que o MTBE é cancerígeno.
Por outro lado, é altamente solúvel em água e pouco adsorvido pelo solo,
migra muito rapidamente até às águas subterrâneas, contaminando zonas
onde é captada a água doméstica. A sua utilização tem vindo, por isso,
a ser abandonada. Em Portugal, ainda se usa, nas gasolinas Super Sem
Chumbo 98 e Super Aditivada que contêm cerca de 4% de MTBE.
Entre estas barreiras contam-se[6.9]:
-
A escassez de terra disponível. Para adicionar 5% do etanol à gasolina
consumida em Portugal, seriam necessários cerca de 500000ha de terra,
consoante o tipo de matéria-prima considerada. Desde as imposições da
PAC, apenas 10% das terras estão em pousio. -
Baixa produtividade agrícola: 0,7 ton/ha em Portugal, face a 1,3 em
Espanha e 2 em França e Itália. Isto implica que em Portugal o biocombustível
fique mais caro do que os combustíveis convencionais. -
Falta de incentivo fiscal, ao contrário do que se passa noutros países
europeus com o biodiesel e nos EUA, Espanha e Suécia com o bioetanol.
6.1 –
Processos Industriais de Produção de Etanol
Feita esta introdução, e antes de mais
para nos situarmos, interessa saber agora quais os processos para a
produção de etanol que se nos apresentam a nível industrial. Existem
essencialmente três:
A) Hidratação Directa do Etileno B) Hidratação Indirecta do Etileno C) Fermentação
Processo
A – Hidratação Directa
A simplicidade reaccional desta via
contrasta vivamente com o nível de complexidade do processo. De facto,
a reacção não podia ser mais simples:
Trata-se de uma reacção bastante exotérmica
(DH2980=-45kJ/mol).
Esta característica, aliada ao facto de se dar um aumento do número
de moles, indicaria que as condições óptimas de operação correspondem
a baixas temperaturas e elevadas pressões (em termos de equilíbrio termodinâmico).
Sucede, no entanto, que boas velocidades de reacção se obtêm nas proximidades
dos 300ºC e 70bar (tempos de residência baixos). A temperatura terá
então de ser elevada, o que limita a taxa de conversão a valores tão
baixos como 4%. Assim sendo, surge a necessidade de reciclar grandes
quantidades de etileno. E como a reciclagem é intensiva, torna-se crítica
a pureza da alimentação de etileno, caso contrário acumular-se-iam gases
inertes. Neste ponto, uma preocupação a ter é a inexistência, na alimentação,
de acetileno (C2H2), que poderia hidratar-se em
acetaldeído. No que respeita a pressão, esta não pode subir muito acima
do valor indicado, sob o risco de se assistir a uma polimerização do
etileno. Esta reacção acelera-se com o auxílio catalítico (geralmente
ácido fosfórico, H3PO4, num suporte de sílica).
A operação conduz-se com um rácio de água para etileno à volta de 0,6.
As matérias iniciais podem ser o petróleo, carvão, ou gás natural.
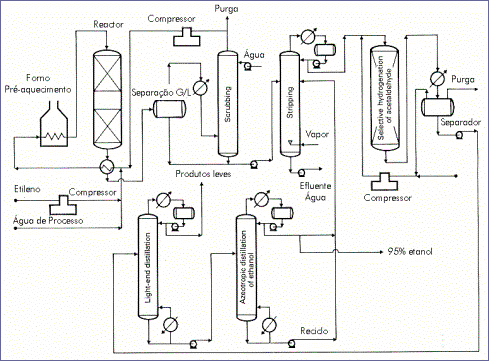
Fig. 6.5 – Produção Industrial
de Etanol por Hidratação Directa do Etileno. [6.1]
Os gases libertados no reactor são
condensados parcialmente, e sofrem um processo de scrubbing onde os
vestígios de ácido fosfórico se neutralizam. Há um segundo arrefecimento,
no qual condensa uma fracção de água/álcool. Depois de outro scrubbing
com água e uma purga, os gases restantes são então comprimidos e reciclados.
A mistura água/etanol é enviada para uma primeira coluna de destilação
para remover componentes leves (éteres), e depois para uma segunda,
onde se destila água e o azeótropo de etanol. Qualquer acetaldeído formado
é convertido a álcool por hidrogenação catalítica com níquel. A selectividade
do etanol em relação ao etileno é de 98,5%.
Processo
B – Hidratação Indirecta
A hidratação indirecta é, dos três
processos, aquele que tem sido abandonado em termos industriais. Baseia-se
numa sequência de dois passos: esterificação e hidrólise. No entanto,
a hidrólise dos ésteres sulfúricos origina, além do etanol, um subproduto:
o éter dietílico, sendo esta uma grande desvantagem.
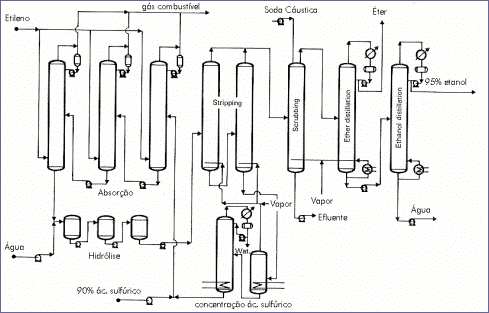
Neste processo, o etileno diluído é
posto em contacto com ácido sulfúrico 98% (w/w), em contracorrente numa
coluna de absorção a 80ºC e a 1,3-1,5bar. A principal impureza do etileno
é etano. A exotermicidade da reacção requer controlo de temperatura,
que é feito com um sistema exterior de arrefecimento, e acompanhado
por uma medição rigorosa dos volumes de reagentes em jogo. Os gases
não absorvidos saem no topo como gases para combustão. Os esteres sulfúricos
e éter dietílico absorvidos são então hidrolisados, e esta quantidade
de água que entra em jogo baixa a concentração do ácido para 50%(w/w).
Os produtos da hidrólise entram depois numa coluna de stripping, que
na sua base direcciona o ácido sulfúrico para um ciclo de recuperação
(concentração feita em evaporadores sob vácuo). Os componentes voláteis
saem do topo da coluna e sofrem um processo de scrubbing com água ou
soda cáustica diluída. O etanol é separado do éter dietílico por fraccionamento.
Fig. 6.6 – Produção Industrial
de Etanol por Hidratação Indirecta do Etileno. [6.1]
Além da presença de um subproduto,
este processo possui outras desvantagens. O uso de ácido sulfúrico é
responsável por inúmeros problemas de corrosão, aos quais se somam os
custos do ciclo de recuperação do ácido, que são um dos maiores encargos
financeiros. Fica então claro o porquê do abandono desta via de produção.
Processo
C – Fermentação
Este é, de facto, dos três processos
o mais antigo. Tão antigo que, apesar da sua aplicação à escala verdadeiramente
industrial datar de 1930, é um dos processos químicos que o Homem mais
cedo descobriu. E se há 30 séculos os chineses destilavam o etanol a
partir de licor fermentado de arroz, hoje em dia a fermentação é o processo
industrial dominante (90% da produção mundial), e faz-se a partir de
uma série de matérias-primas possíveis – açúcares (melaço, cana de açúcar,
beterraba), amidos (milho, trigo, aveia, arroz, mandioca, batata doce,
ervilha, feijão), celuloses (madeira, resíduos industriais ou agrícolas).
Alguns dos microorganismos usados são as Saccharomyces
cerevisiae e Zymonas mobilis.
As reacções em jogo são:
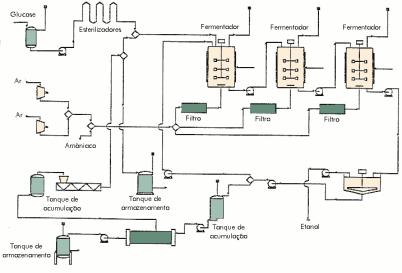
Muito rapidamente, o exemplo de um
processo de fermentação de açúcar é ilustrado na figura abaixo. A produção
faz-se numa bateria de fermentadores que operam em contínuo. A corrente
do 3º fermentador segue para um decantador que recebe a mistura que
contém água, etanol, e óleo. O decantador liberta biomassa e proteínas.
Desta corrente recircula-se 25% para o primeiro fermentador. Os restantes
75% são enviados para um filtro prensa que produz um composto rico em
proteínas, o DDGS, que é vendido como ração animal. [6.2]
Fig. 6.7 – Produção Industrial
de Bioetanol por Fermentação. [6.2]
|
[
Custos e Impactes Ambientais no Projecto de Processos Químicos ]
[
Âmbito do Trabalho ]
[ Enquadramento da Questão Ambiental ]
[ Indicadores para Análise Ambiental ]
[
Ferramentas para Análise Ambiental de Processos Químicos
] [ Projecto de Caminhos
Reaccionais ]
[
CASE STUDY - Produção de Etanol ]
[ Conclusões ]
[ Nomenclatura ]